はじめに
経口固形投与(OSD)製造は、依然として製薬業界で最も広く使用され、商業的に重要な医薬品製造形態の1つです。市販の鎮痛剤から複雑ながん治療まで、錠剤やカプセルは現代医学の基礎となっています。一見簡単そうに見えますが、経口固形分を大規模に製造するには、製品の一貫性、品質、規制遵守を確保するためには驚異的な精度が必要です。
しかし、製薬メーカーは一貫した生産量を達成する上で、依然として大きな課題に直面しています。乾式造粒や混合などのプロセス中に生じるばらつきは、最終製品の有効性、バイオアベイラビリティ、保存期間を損なう可能性があります。このような不一致は、治療結果に影響するだけでなく、厳格なGMP規制のもとでは、費用のかかるリコールや生産停止の原因にもなります。1
プロセスのばらつきを減らし、品質管理を改善し、一貫した品質成果を維持しようとする製薬メーカーにとって、人工知能(AI)とデジタルツインが鍵となりつつあります。AI は、従来のデータモニタリングからリアルタイムの予測や実行可能な推奨事項へと移行することで、安全で一貫性のある信頼性の高いOSD製造の新時代の到来を告げています。
OSD製造における不整合の根本原因
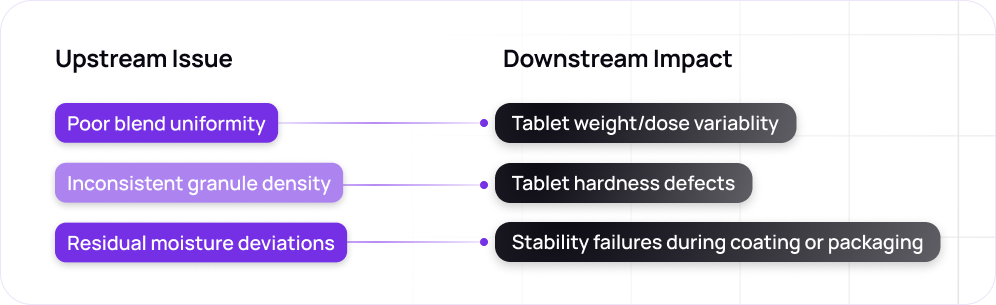
製品の品質に影響する変数が非常に多いため、OSD製造における均一性の実現は複雑です。こうした不一致は、多くの場合、上流の原材料や合成などの初期プロセス段階で発生し、積極的に対処しなければ下流の問題に発展する可能性があります。
原材料のばらつきが主な原因です。同じ材料を使って作業している場合でも 医薬品有効成分 (API) また、添加剤の場合、粒度分布、含水率、流動性、またはかさ密度のわずかな違いが、ブレンドの均一性と圧縮挙動に大きな影響を与える可能性があります。2 これらの物理的属性は、サプライヤー、ロット、または保管条件によって変わる可能性があるため、従来のツールを使用してその影響を予測することは困難です。
プロセスの偏差は、一貫性の欠如のもう1つの重大な原因です。OSD製造では、造粒、混合、錠剤化、コーティングなど、緊密に連携した一連のユニット操作が必要であり、それぞれが最終製品の品質にばらつきをもたらす可能性があります。
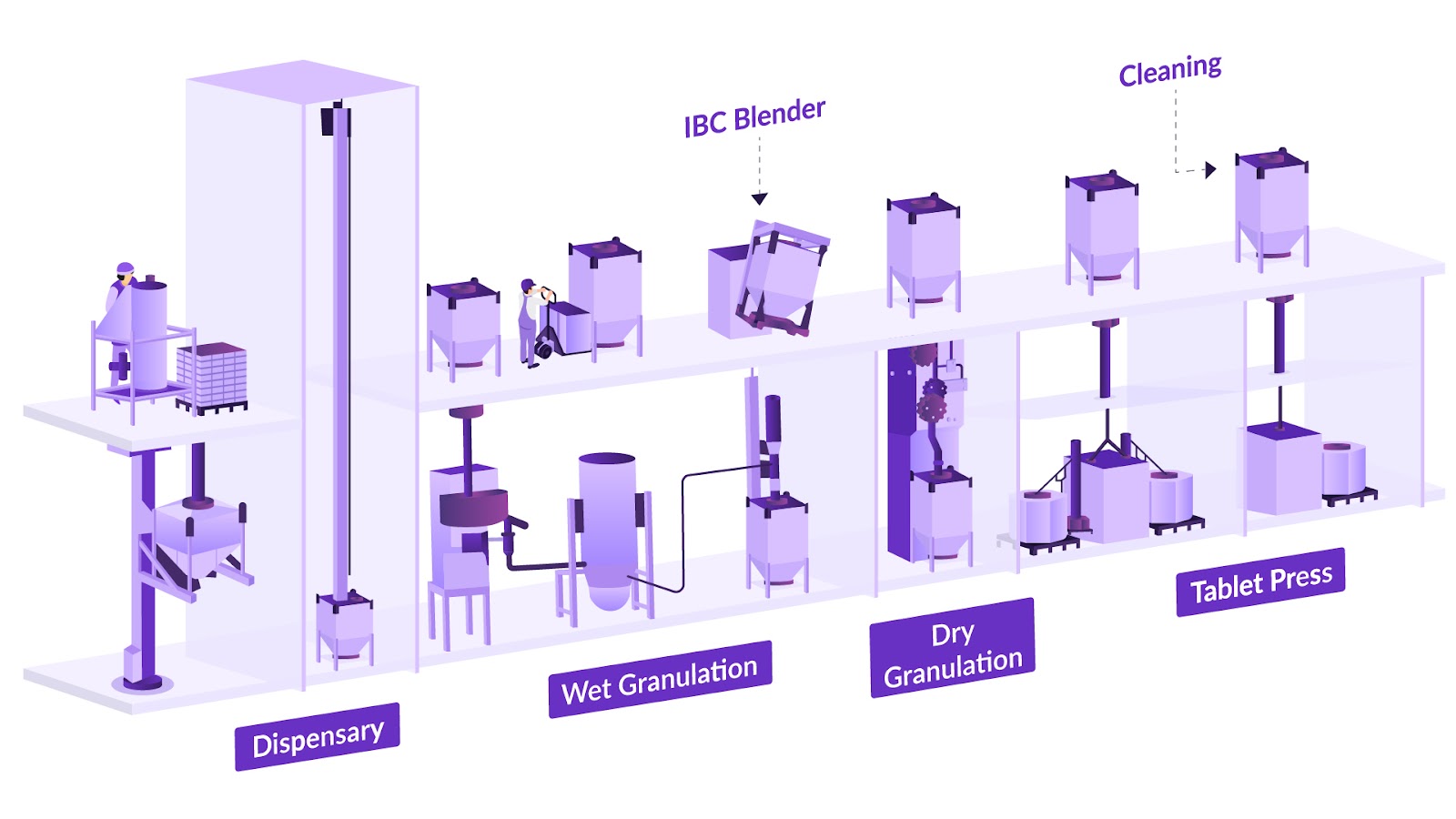
たとえば、造粒はバインダー濃度、せん断力、乾燥条件などの要因の影響を受けますが、これらはすべて最終的な顆粒のサイズと水分レベルに影響します。3 ブレンドは分離の影響を受けやすく、ブレンドの均一性が低いと、下流のOSDプロセスで錠剤の投与量が変動する可能性があります。4 コーティングプロセスは噴霧速度と均一性に依存するため、システム全体がどの段階でも変動の影響を受けやすくなります。
「プラグフロー」(均一性に不可欠)を維持するには、機器を材料特性に合わせて正確に調整する必要があるため、連続処理はこれらの課題をさらに悪化させる可能性があります。4
従来のデータ主導型のアプローチは、レトロスペクティブ分析には役立ちますが、多くの場合、このレベルの変動にリアルタイムで対処するには不十分です。このような多変量モデル (MVAなど) は、「ゴールデンバッチ」の軌跡を捉えることができても、推奨値を示さなかったり、偏差が検出されたときに自動的にセットポイントを調整したりすることはできません。さらに、これらのデータ駆動型モデルはしばしば「ブラックボックス」であり、偏差やその他の品質問題の根本原因に関するエンジニアリング上の「説明可能性」はありません。
言い換えると、現在採用されている既存のアプローチでは、メーカーは問題について警告を受けても、規制当局やエンジニアが理解して受け入れることができる方法で問題を解決する方法についての明確なガイダンスがないことがよくあります。
現在のOSDマニュファクチャリングの現状
自動化とPAT(プロセス分析技術)の進歩にもかかわらず、多くの製薬会社は依然としてセグメント化されたデータシステム、レガシー機器、事後対応型の品質管理プロトコルを使用して事業を行っています。
バッチが仕様を満たさない場合、根本原因の調査は多くの場合、手作業によるデータ集約と試行錯誤による調整に頼ります。このような事後対応型のアプローチは、ダウンタイムの長期化、利回りの損失、潜在的なコンプライアンスリスクにつながる可能性があります。5
現代のOSD製造には、よりプロアクティブで予測的なフレームワークが必要であるという認識が高まっています。つまり、結果を事前にシミュレートし、最適な進路を推奨し、プロセスデータから継続的に学習できるフレームワークです。
OSD 製造におけるばらつきを減らすための AI アプリケーション
AIは、OSD製造プロセス全体のばらつきの根本原因に対処することにより、変革的なアプローチを導入します。真のプロセスデジタルツインは、記述的分析だけに頼るのではなく、履歴データやリアルタイムデータから継続的に学習し、結果をシミュレートし、品質とパフォーマンスの目標に沿った変更を推奨することができます。
プロセスシミュレーション用の AI 対応デジタルツイン
デジタルツインは物理プロセスをリアルタイムで仮想的に表現したもので、OSD製造では、さまざまな条件下での造粒機、ブレンダー、タブレットプレス、コーターの動作を模倣します。これらの AI 対応システムにより、製造業者は生産を中断することなく「もしも」のシナリオをシミュレートするなど、さまざまなアプリケーションを実現できます。ハイブリッドデジタルツインモデルでは、物理学の原理とデータ主導型のアプローチを組み合わせてモデルの精度を向上させることで、シミュレーションをさらに進めることができます。
たとえば、混合プロセスのデジタルツインでは、インペラーの速度やブレンド時間の変化が、バッチ全体の API 分布の均一性にどのように影響するかをシミュレートできます。オペレーターは、ブレンド後のアッセイ結果に頼って分離や内容の均一性の問題を特定する代わりに、これらの予測的知見を活用して積極的にパラメーターを調整し、生産開始前に一貫したブレンド品質を確保することができます。6
モデルベースのシミュレーションは粉体混合ダイナミクスの理解を大幅に深め、試行錯誤による方法への依存を減らし、バッチの一貫性を向上させることができることが研究によって示されています。7
デジタルツインは、スケールアップと技術移転に特に役立ちます。これにより、チームは一貫性のないリスクを最小限に抑えながら、機器や製造現場全体でプロセス調整をテストできます。
リアルタイムのプロセス監視と最適化
OSD製造におけるAIの最も強力な用途の1つは、プロセスをリアルタイムで監視、予測、最適化できることです。デジタルツインと AI オプティマイザーを組み合わせることで、センサー (PAT ツール、MES システムなど) からデータを取り込んで、逸脱の兆候を早期に検出し、問題が製品の品質に影響する前にプロセスの設定値を調整するための推奨事項を提示できます。
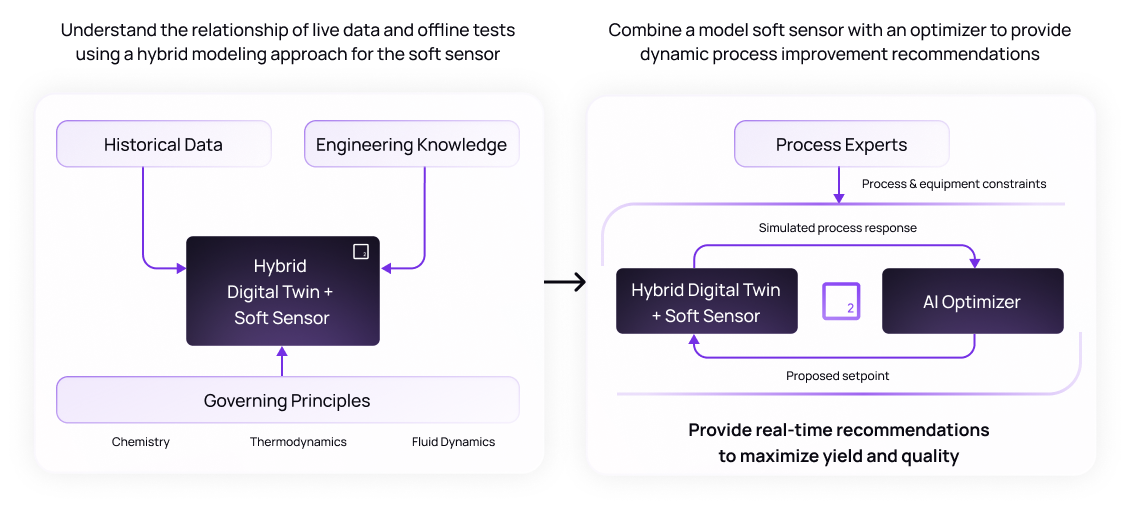
従来の制御システムとは異なり、AIは異常を通知するだけでなく、現在の状況に合わせた設定値の調整やプロセス介入を推奨します。例えば、 Basetwoによる1つのユースケースでは 造粒水分がデジタルツインで特定された望ましい範囲から外れる傾向が始まり、AIシステムが乾燥空気の温度と流量の変更を提案して問題を修正します。8
このように事後管理から規範的制御に移行することで、プロセスの信頼性が向上し、原材料のばらつきや機器の摩耗が発生した場合でも、各段階が重要な品質属性内にとどまることが保証されます。
結論
経口固形製剤の一貫性を維持することは、規制上の義務であると同時にビジネス上必要でもあります。品質とコンプライアンスが懸かっているため、製薬メーカーは、予測が限られ対応が遅れる従来のツールに頼る余裕がなくなりました。
AIとデジタルツインのアプローチは根本的に異なります。つまり、予測的洞察、リアルタイムモニタリング、規範的制御を組み合わせて変動を根本的に減らすというアプローチです。
デジタルツインやAIなどの最新テクノロジーを採用することで、OSDメーカーは今日の生産需要を満たすだけでなく、ますます複雑化する規制や競争環境の中で長期的な成功を収めることができるようになります。
AIがOSDプロセスにどのように影響するかを調べるには、 デモを予約 今日はベースツーで!
参考文献:
- 米国食品医薬品局(2021)。業界向けガイダンス:プロセス検証:一般原則と実践。https://www.fda.gov/media/71021/download
- チャオ・ユイ他(2020)。錠剤製造における配合の均一性に対する原薬および添加剤のばらつきが及ぼす影響 国際製薬ジャーナル、586、19564。
- シン、R.、他(2019)。医薬品造粒におけるプロセスの理解と制御:レビュー パウダーテクノロジー、356、478-495。
- ダビラ、H.T.(2013年4月16日)。 連続OSD製造を最適化する方法。医薬品製造。https://www.pharmamanufacturing.com/facilities/op-ex-lean-six-sigma/article/11357740/pharma-industry-how-to-optimize-continuous-osd-manufacturing-pharmaceutical-manufacturing
- クマール、A.、他(2021)。医薬品製造におけるリアルタイムリリーステストと AI の導入における課題 製薬イノベーションジャーナル、16、155-167。
- ユアン、Y.-S.(2023年7月25日)。 連続医薬品製造のためのデジタルツイン開発と高度なプロセス制御. figshare。https://hammer.purdue.edu/articles/thesis/Digital_Twin_Development_and_Advanced_Process_Control_for_Continuous_Pharmaceutical_Manufacturing/23735379%C2%A0
- ガルシア・ムニョス、S.、ボナム、R.、ゴヤル、S.(2020)。 医薬品の開発と製造におけるデジタルツインの応用。APS ジャーナル、2 (5)、1—10。
- 医薬品製造:ベースツーエイド。医薬品製造 | ベースツー人工知能(n.d.). https://www.basetwo.ai/pharmaceuticals



